Regeneracja tkanki jajnika
Przedwczesna niewydolność jajników (POI) dotyka od 1% do 3,7% kobiet w wieku rozrodczym. Stan ten charakteryzuje się występowaniem objawów typowych dla menopauzy poniżej 40 roku życia, przy jednoczesnym wzroście FSH i niewykrywalnym poziomie AMH w surowicy krwi. Biorąc pod uwagę fakt, że menopauza w populacji kaukaskiej występuje średnio w wieku 51,4 lat, jest to znaczące skrócenie biologicznej funkcji jajników jako gruczołów dokrewnych u ludzi. Obecnie istnieją dwie główne teorie wyjaśniające etiologię choroby: czynniki genetyczne odpowiedzialne za przedwczesne wyczerpanie rezerwy jajnikowej, z towarzyszącym zwiększonym ryzykiem raka i skróceniem długości życia; choroby autoimmunologiczne – gdy przeciwciała przeciwko gruczołom dokrewnym przenikają do płynu pęcherzykowego i uszkadzają oocyty. Leczeniem pacjentek z POI jest hormonalna terapia zastępcza. U pacjentek, które chcą zostać matkami, dawstwo oocytów jest leczeniem z wyboru.
Mezenchymalne komórki macierzyste to komórki multipotencjalne, które mają zdolność do różnicowania się i dojrzewania w komórki chrząstki, kości i tłuszczu oraz mogą pomagać i wchodzić w interakcje z innymi komórkami macierzystymi. Mają one również zdolność do modulowania niektórych elementów układu odpornościowego. Mezenchymalne komórki macierzyste charakteryzują się zdolnością do samoodnawiania i różnicowania się w chrząstkę, kość i tłuszcz, do przylegania i wzrostu in vitro. Mezenchymalne komórki macierzyste mogą mieć różne pochodzenie. Można wyróżnić embrionalne mezenchymalne komórki macierzyste, płodowe komórki macierzyste – ze sznura pępowinowego i galarety Whartona oraz dorosłe mezenchymalne komórki ze szpiku kostnego i tkanki tłuszczowej.
Mezenchymalne komórki macierzyste pochodzące z galarety Whartona spełniają opisane powyżej kryteria: są samoodnawiające się i mogą różnicować się w różne tkanki, nie tylko kości, chrząstki i tłuszcz, ale także w:
- komórki mięśni poprzecznie prążkowanych,
- kardiomiocyty,
- hepatocyty,
- komórki Langerhansa trzustki,
- komórki nerwowe.
Mogą również brać udział w regeneracji struktur siatkówki. Na swojej powierzchni posiadają antygeny zgodności tkankowej typu I (HLA – I), nie posiadają natomiast markerów powierzchniowych antygenów HLA typu II. Powyższe właściwości immunologiczne tych komórek skutkują zarówno brakiem odpowiedzi immunologicznej na przeszczep komórek mezenchymalnych od innego dawcy, jak i brakiem rozpoznawania przez allogeniczne komórki mezenchymalne biorcy jako struktur obcych. Uważa się, że mezenchymalne komórki macierzyste działają jako lokalny koordynator naprawy tkanek. Naprawa uszkodzonej tkanki odbywa się poprzez regulację endogennych procesów regeneracyjnych, a nie poprzez zastępowanie uszkodzonej tkanki strukturami de novo.
Płodowe MSC mają większy potencjał ekspansji w hodowli in vitro niż dorosłe mezenchymalne komórki macierzyste. Wielu autorów uważa, że jest to konsekwencją dwóch przejść pierwotnych komórek krwiotwórczych z zarodka do struktur łożyska i z powrotem. Najpierw między 4 a 12 dniem embriogenezy przez prymitywną pępowinę komórki krwiotwórcze migrują z woreczka żółtkowego do łożyska. Następnie, podczas drugiej migracji, MSC są przekazywane w przeciwnym kierunku. Z łożyska wracają ponownie do płodu: do wątroby, a następnie do szpiku kostnego. Naukowcy postawili hipotezę, że podczas tej migracji komórki mezenchymalne w galarecie Whartona zostają „uwięzione” od wczesnej embriogenezy, przez cały okres ciąży, aż do porodu.
Ostatnie odkrycia dokonane w dziedzinie pochodzenia i rozwoju komórek macierzystych dowodzą, że pierwotne komórki zarodkowe (PGC) i ich depozyty, pozostające w rozwijających się tkankach organizmu – bardzo małe embrionalne komórki macierzyste (VSEL) – odgrywają kluczową rolę w procesie regeneracji. Niektóre wcześniejsze badania sugerują, że pierwotne komórki macierzyste (bardzo małe MSC zdeponowane w takcie jajnika), przechodzą asymetryczne podziały komórkowe i są w stanie wytwarzać oogonalne/zarodkowe komórki macierzyste, a te ostatecznie oocyty. Czynnikiem stymulującym vsMSCs do podziałów mogą być mezenchymalne komórki macierzyste i wytwarzane przez nie egzosomy. W modelach zwierzęcych wykazano, że stymulacja pierwotnych komórek macierzystych do produkcji oocytów jest w stanie przywrócić hormonalną i prokreacyjną funkcję jajników uprzednio uszkodzonych przez radio- i chemioterapię. Sugeruje to, że analogiczne korzyści powinny odnieść kobiety, u których rozwinęło się POI.
DeCure
Doświadczenia własne
Prace badawcze z wykorzystaniem mezenchymalnych komórek macierzystych (MSC) u pacjentek z przedwczesną niedoczynnością jajników (POI), prowadzimy od 2016 r.
Mamy doświadczenie z wykorzystaniem komórek macierzystych pozyskanych z galarety Wharton’a, tkanki tłuszczowej oraz ze szpiku kostnego.
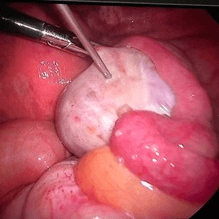
Materiał biologiczny w trakcie laparoskopii, podajemy bezpośrednio do tkanki jajnika.
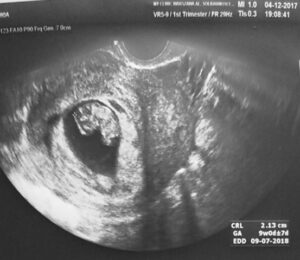
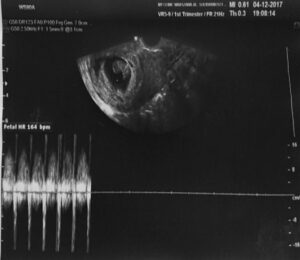
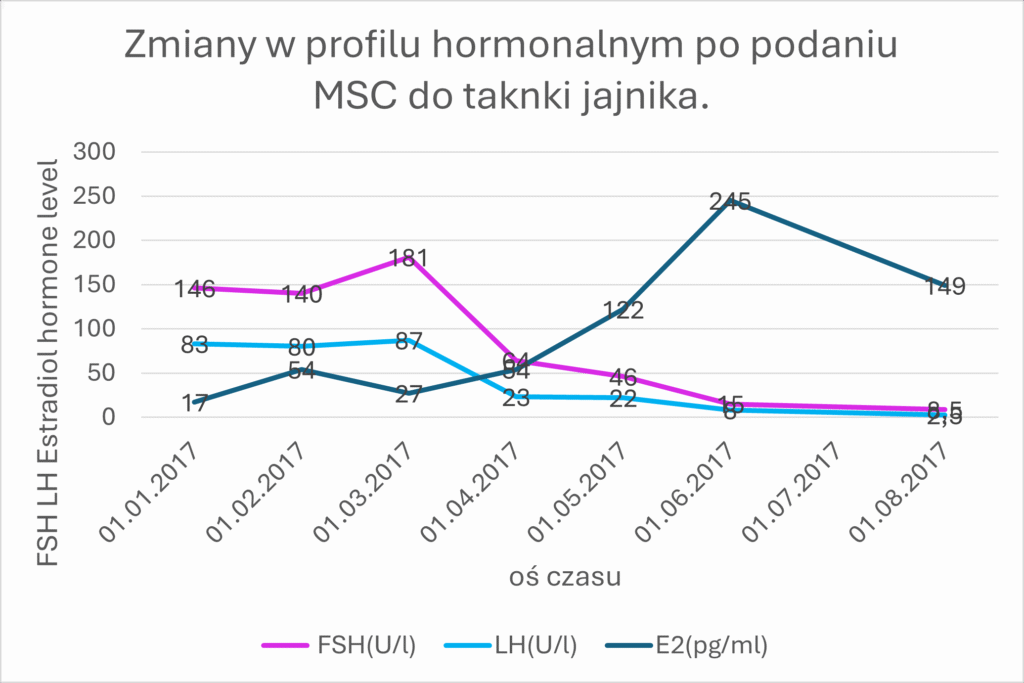
Zastosowanie MSC ze sznura pępowiny, pozwoliło na przywrócenie funkcji hormonalnej oraz prokreacyjnej w tkance jajnika. Efekt biologiczny mierzony jako wartość stężenia hormonów płciowych w surowicy krwi u pacjentek po podaniu materiału biologicznego obserwujemy po okresie od 3 do 6 miesięcy. Na wykresie przedstawiono wyniki 35 letniej pacjentki z przedwczesną menopauzą (FSH 146 U/l, LH 83 U/l, E2 17 pg/ml). Po podaniu komórek macierzystych nastąpił powrót do prawidłowych wartości hormonów płciowych (FSH 2,5 U/l, E2 149 pg/ ml)
Zmiany obserwowane są także w takcie badania USG dopochwowego.
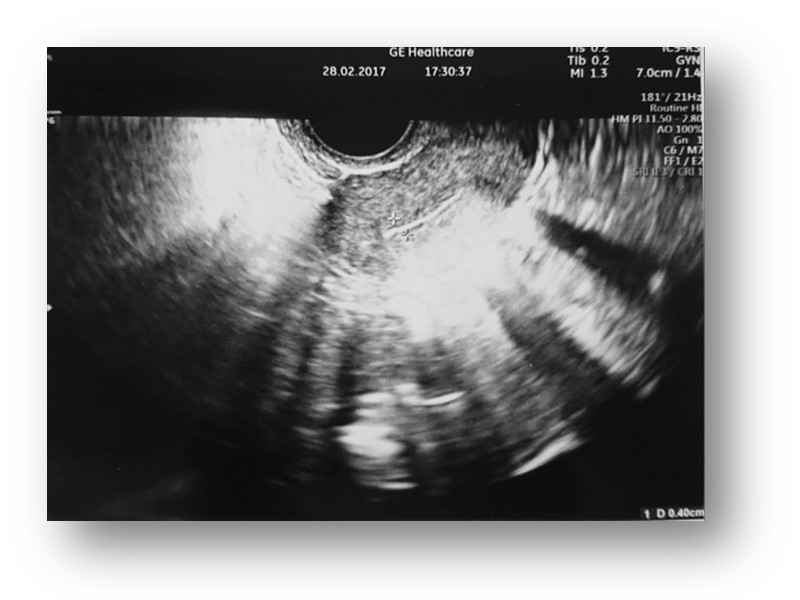
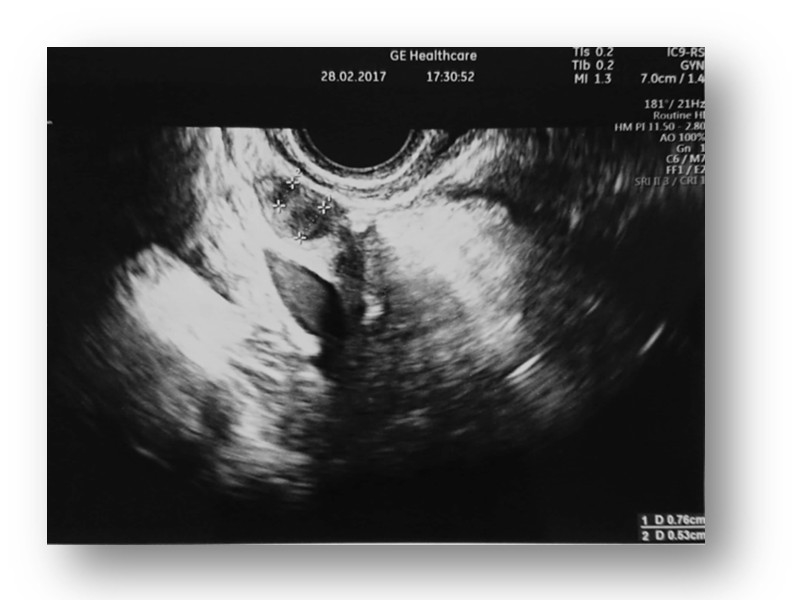
Obraz USG TV macicy wraz endometrium oraz jajnika przed podaniem MSC.
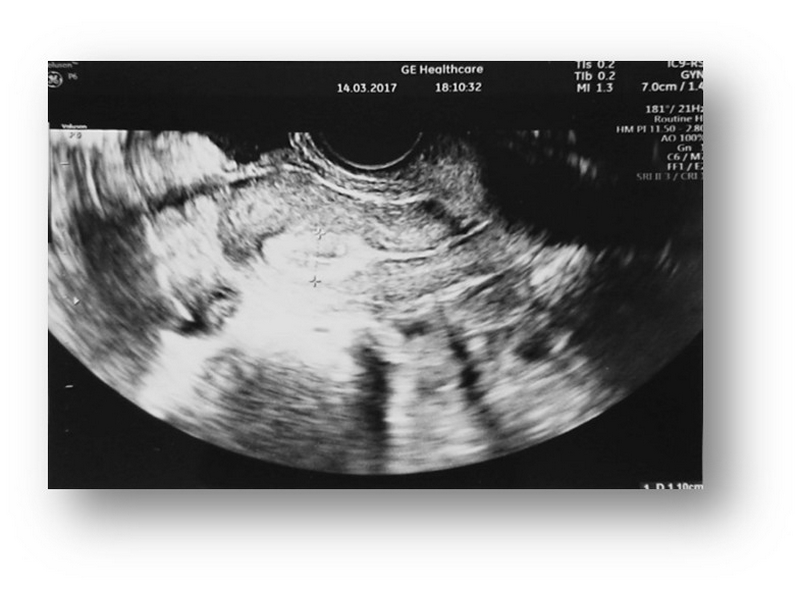
Obraz USG TV macicy wraz endometrium oraz jajnika po podaniu MSC.
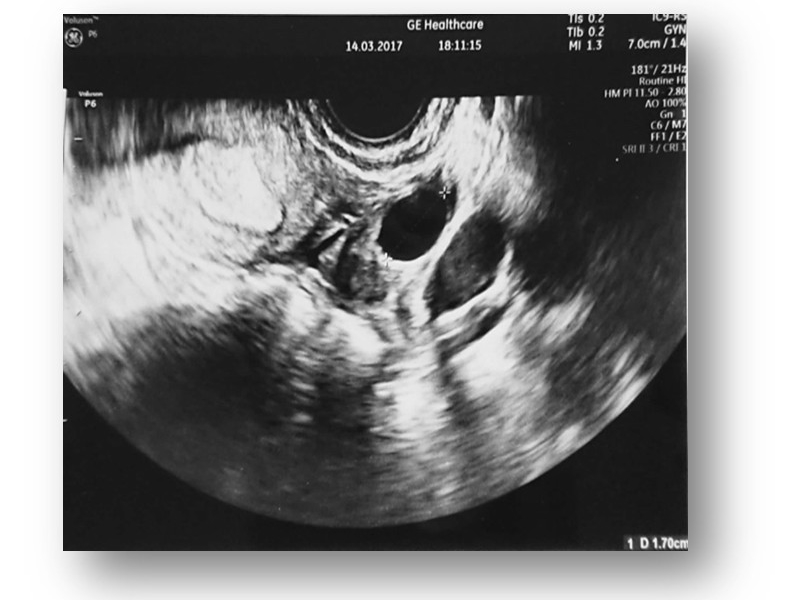
Szansę na uzyskanie ciąży, pacjentki mają
zarówno w programie IVF


Blastocysta – zarodek w 5 dobie życia
jak i w wyniku
spontanicznego poczęcia,